





人教版 (新课标)选修2 化学与技术课题2 海水的综合利用说课课件ppt
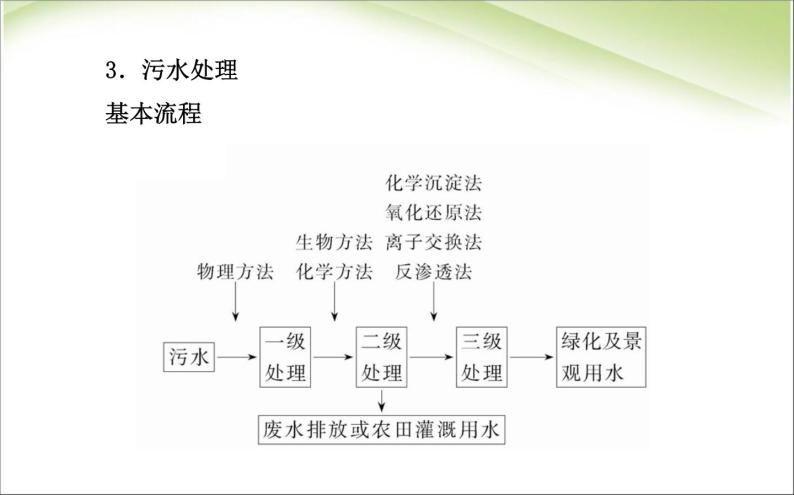
展开一、获取洁净的水1.水的净化(1)基本流程:
①常用的混凝剂有:_____、_________、_____、聚合铝等。②常用的消毒剂有:_______、_____、ClO2、高铁酸盐等。(2)明矾净水原理:明矾在水中发生电离:____________________________,Al3+发生水解:_________________________________,氢氧化铝胶粒能破坏天然水中的胶体杂质的稳定性,吸附悬浮物而沉降。
2.硬水的软化(1)硬水和软水: 硬水:含_________较多的水 软水:含少量或不含_________的水(2)硬水的类型:暂时硬度——由钙、镁的_________引起的硬度永久硬度——由钙、镁的_______________引起的硬度(3)硬水的软化方法:硬水软化的常用方法有_______、药剂法和离子交换法等。
二、海水的综合利用1.海水水资源的利用——海水淡化海水淡化的常用方法有_______、电渗析法和离子交换法等。
2.海水中化学资源的开发利用(1)海水中食盐的开发利用:①海水制盐从海水中提取食盐的主要方法是_______。其原理是将海水太阳照射后,蒸发浓缩,使食盐结晶析出。得到的产品为粗盐。另外还有电渗析法和冷冻法。②氯碱工业a.原料:粗盐b.反应原理:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
c.工艺流程d.设备:离子交换膜电解槽。
(2)从海水中提取镁:生产流程及反应原理
CaO+H2O====Ca(OH)2
MgCl2+Ca(OH)2==== Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl2====MgCl2+2H2O
(3)从海水中提取溴:
反应原理氯化:______________________①____________________________________,_______________________________________。②__________________________,_____________________。
Cl2+2NaBr====2NaCl+Br2
3Br2+3Na2CO3 ==== 5NaBr+NaBrO3+3CO2↑
5NaBr+NaBrO3+3H2SO4====3Br2+3Na2SO4+3H2O
Br2+SO2+2H2O====2HBr+H2SO4
Cl2+2HBr====2HCl+Br2
三、煤、石油、天然气的综合利用1.煤的综合利用
3.煤化工和天然气化工的发展——一碳化学(1)煤的气化:2C+O2 2COC+H2O CO+H2CO+H2O CO2+H2(2)天然气的利用:①CH4+H2O CO+3H2②2CH4+O2 2CH3OH
【思考辨析】1.硬水中加入适量石灰水后,由于生成Mg(OH)2、CaCO3沉淀,水就软化了。( )【分析】加入石灰水后,只能将Mg2+引起的硬度转化为Ca2+引起的硬度,仍然存在大量的Ca2+。2.废水中的重金属离子Hg2+、Pb2+、Cu2+均可用加入强碱(NaOH)使其沉淀的方法除去。( )【分析】Hg2+、Pb2+、Cu2+等重金属离子应用Na2S使其转化成硫化物沉淀而除去。
3.离子交换膜电解槽电解食盐水时阴极产物是NaOH和氢气。 ( )【分析】电解食盐水时,阳极产物是Cl2,阴极产物是H2和NaOH。4.将MgCl2·6H2O加热分解可制得无水氯化镁。( )【分析】MgCl2·6H2O加热时MgCl2发生水解,生成Mg(OH)2,故应在HCl的气流中加热MgCl2·6H2O才能得到无水MgCl2。5.石油裂化的目的是为了获得以短链不饱和烃为主要成分的基本化工原料。( )【分析】石油裂化的目的是为了提高轻质油的产量,而裂解的主要目的是为了获得短链的不饱和烃。
6.石油的分馏和煤的干馏都是物理变化过程。( )【分析】石油的分馏是物理变化,而煤的干馏是化学变化。7.从海水中提取溴的工艺流程中有两次由Br-→Br2的目的是提高溴的产量。( )【分析】第一次由Br- Br2的目的是富集海水中的溴。第二次是为了提纯Br2。因为第一次得到的Br2中混有水,不易分离,使其转化为Br-,再氧化得Br2。
考点 1 氯碱工业 1.原料精制饱和食盐水。(1)精制目的:除去泥沙,使Ca2+、Mg2+、Fe3+、S 等离子的含量达到要求。(2)精制原因:Ca2+、Mg2+等在碱溶液中形成的沉淀及泥沙等会破坏离子交换膜,而使产品不纯。
(3)精制方法:用BaCl2除去 用Ca(OH)2除去Mg2+、Fe3+,用Na2CO3除去Ba2+及Ca2+,所加沉淀剂需稍过量。最后加盐酸调节盐水的pH。
(4)有关离子方程式:Ba2++ ====BaSO4↓Mg2++2OH-====Mg(OH)2↓Fe3++3OH-====Fe(OH)3↓Ca2++ ====CaCO3↓Ba2++ ====BaCO3↓ +2H+====H2O+CO2↑
(5)工艺流程:粗盐水 过滤 离子交换树脂→精盐水。在进入电解槽前需通过离子交换树脂进一步除去Ca2+、Mg2+等离子,以防破坏离子交换膜。2.原理2NaCl+2H2O 2NaOH+H2↑+Cl2↑
3.主要设备离子交换膜电解槽:阳极室:加入的是精制后的饱和食盐水阴极室:加入纯水(加入一定量的NaOH溶液)
【高考警示】(1)除去饱和食盐水中的Ca2+、Mg2+、S 时,纯碱应在钡试剂之后加入,稀盐酸应在过滤后加入。(2)电解饱和食盐水时要使用惰性电极而不能使用Fe、Cu等活性电极,否则阳极得不到Cl2。(3)阳离子交换膜既防止了Cl2与NaOH溶液的反应,又防止了Cl2与H2的反应。
【典例1】(2012·浙江高考)(1)氯碱工业是利用电解食盐水生产 ① 为基础的工业体系。(2)电解前,为除去食盐水中的Mg2+、Ca2+、S 等杂质离子,下列加入顺序合理的是 ② 。A.碳酸钠、氢氧化钠、氯化钡B.碳酸钠、氯化钡、氢氧化钠C.氢氧化钠、碳酸钠、氯化钡D.氯化钡、氢氧化钠、碳酸钠
(3)“盐泥”是粗盐提纯及电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
为了生产七水硫酸镁,设计了如图所示的工艺流程:
装置1中加入的酸应选用 ③ ,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是 ④ 。装置2中滤渣的主要成分为 ⑤ 。装置3中通入高温水蒸气并控制温度在100℃~110℃,蒸发结晶,此时析出的晶体主要是 ⑥ 。用装置6(真空干燥器)干燥七水硫酸镁晶体的理由是 ⑦ 。
【解题指南】解答本题要注意以下2点:(1)关注“盐泥”的主要成分。(2)粗盐的提纯过程中试剂的滴加顺序。
【解析】(1)由于电解饱和食盐水的过程中产生了Cl2、H2和NaOH,所以电解食盐水主要是为了制取以上三种物质。(2)在粗盐提纯过程中,所加除杂试剂的顺序通常为先加BaCl2,再加NaOH,最后加入Na2CO3。加NaOH的顺序可以放在BaCl2的前面也可以放在Na2CO3的后面,但Na2CO3的加入顺序必须放在BaCl2的后面,因过量的BaCl2需用Na2CO3除去。(3)由于最终的产品为MgSO4•7H2O,所以所加的酸应该是H2SO4,加入H2SO4后发生的反应有:Mg(OH)2+H2SO4====MgSO4+2H2O,CaCO3+H2SO4====CaSO4+CO2↑+H2O。CaCO3和H2SO4的反应之所以能够持续进行,是因为
该反应是在50℃及持续搅拌的条件下进行的,该条件下CO2可以迅速从溶液中逸出而使平衡不断向正反应方向移动。CaSO4是一种微溶物,滤渣中除BaSO4、不溶于酸的物质外还应含有CaSO4。在真空干燥器中MgSO4·7H2O表面的水不需要加热烘干就能挥发掉,这样就能有效防止失去结晶水。
答案:①氯气、烧碱、氢气(只写出氯气、烧碱也可)②D ③(稀)硫酸④搅拌过程中CO2不断逸出,使平衡CaCO3+H2SO4 CaSO4+H2CO3,H2CO3 H2O+CO2↑不断向右移动⑤CaSO4、BaSO4、其他不溶于酸的物质⑥氯化钠 ⑦防止失去结晶水
【互动探究】电解前除去食盐水中的Mg2+、Ca2+、S 等杂质离子,除本题的(2)中的试剂加入顺序外,还有其他加入顺序吗?提示:还可以按以下顺序除去食盐水中的杂质离子:NaOH→BaCl2→Na2CO3
考点 2 水的净化与处理 1.硬水软化的方法(1)加热法(只能软化具有暂时硬度的水):其原理为Ca(HCO3)2 CaCO3↓+CO2↑+H2O,Mg(HCO3)2 MgCO3↓+CO2↑+H2O,继续煮沸时,MgCO3可转化为更难溶的Mg(OH)2:MgCO3+H2O Mg(OH)2↓+CO2↑。
(2)药剂法(石灰纯碱法):反应原理:①Ca(HCO3)2+Ca(OH)2====2CaCO3↓+2H2OMg(HCO3)2+2Ca(OH)2==== 2CaCO3↓+Mg(OH)2↓+2H2OMgSO4+Ca(OH)2====Mg(OH)2↓+CaSO4②Ca2++ ====CaCO3↓
(3)离子交换法:利用了离子交换反应原理,软化水的质量高。常用离子交换树脂作离子交换剂,其软化硬水和再生的过程如图所示:
2.污水处理的常用方法
【高考警示】(1)用药剂法软化硬水时一定要注意加入试剂的先后顺序,即Na2CO3应在Ca(OH)2之后加入。(2)用阳离子交换树脂HR除去硬水中的Ca2+、Mg2+时,溶液中的酸性会增强,应再用碱性溶液中和H+。(3)污水处理中的酸性废水常用熟石灰中和而不用NaOH溶液中和,碱性废水常用CO2中和。
【典例2】(2011·山东高考)水处理技术在生产、生活中应用广泛。(1)含有较多 离子的水称为硬水。硬水加热后产生碳酸盐沉淀的离子方程式为:_________________(写一个即可)。(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应该先使硬水通过 (填“RH”或“ROH”)型离子交换树脂,原因是_________________________________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为_______________________。电渗析法净化水时,使离子通过半透膜的推动力是________。(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的__________________________________。
【解题指南】解答本题时注意如下3点:(1)硬水应先通过“RH”,再通过“ROH”,防止生成Mg(OH)2影响交换效果;(2)电渗析法净化水时使离子通过半透膜的推动力是电势差(或电场力)。(3)水是一种极弱的电解质,纯度越高电导率越小或电阻率越大。
【解析】(1)含有较多的钙、镁离子的水称为硬水;加热硬水产生碳酸盐的化学方程式为Ca(HCO3)2 CaCO3↓+CO2↑+H2O;Mg(HCO3)2 MgCO3↓+CO2↑+H2O,故离子方程式为Ca2++ CaCO3↓+CO2↑+H2O;Mg2++ MgCO3↓+CO2↑+H2O。(2)先通过阳离子交换树脂RH,因溶液中镁离子易与ROH型阴离子交换树脂反应生成Mg(OH)2影响交换效果。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,获得纯净水的方法称为反渗透法。电渗析法净化水时,使离子通过半透膜的推动力是电势差(或电场力)。(4)水越纯,电导率越小或电阻率越大,可用于测定水的纯度。
答案:(1)钙、镁Ca2++ CaCO3↓+CO2↑+H2O;(或Mg2++ MgCO3↓+CO2↑+H2O)(2)RH 先通过阴离子交换树脂可能产生Mg(OH)2等沉淀而影响树脂交换效果(3)反渗透法 电势差(或电场力)(4)电导率或电阻率
【互动探究】(1)用蒸馏的方法可得到软水吗?提示:可以,水中钙、镁的化合物难挥发,水蒸气冷凝得到的水属于软水。(2)用RH型阳离子交换树脂软化后的硬水,pH会发生什么变化?只用RH阳离子交换树脂软化的水可用于工农业生产吗?提示:水的pH会减小,酸性增强,不能直接应用于工农业生产。
1.(2012·山东高考)石油和煤炭加工过程涉及多种技术和设备。(1)石油分馏时,在不断向 (填工业设备名称)内投放原料的同时获得产品,该过程为 操作过程。(2)石油裂化分为热裂化、 和加氢裂化,裂化的目的是提高 的产量。(3)煤的洗选是为了降低原煤中灰分和 的含量。煤的流化床燃烧是指空气从底部吹向煤炭颗粒,并使全部煤炭颗粒_______进行燃烧的过程。
(4)煤的直接液化是煤与适当溶剂混合后在高温和 存在下与 作用生成液体燃料的过程。
【解析】(1)石油分馏是在分馏塔中进行的。因石油成分复杂,随分子中碳原子数增加、沸点升高,逐渐分离出沸点在不同范围的馏分。(2)石油裂化分为热裂化、催化裂化和加氢裂化。裂化是将长链烃断为短链烃(轻质油)。(3)煤洗选是降低灰分和硫,可以防止煤燃烧导致酸雨。空气从底部吹入,可使煤粉呈“沸腾”状,燃烧充分。(4)煤的直接液化是煤在催化剂条件下,与H2作用生成甲醇等液体燃料的过程。
答案:(1)分馏塔 连续(2)催化裂化 轻质燃料油(或汽油)(3)硫(S) 浮动(4)催化剂 氢气(H2)
2.水是生命之源,但随着工业的发展,许多宝贵的水资源受到了污染。下面是对某自来水厂水源进行水质分析时得到的部分信息:水体浑浊,有一定异味,pH为6.5,细菌总数1 mL水中含有250个(国家标准规定每亳升不得超过100个)。(1)为了达到饮用水标准,下列处理措施中不正确的是______。A.加混凝剂沉降 B.用碱调节到中性C.用活性炭吸附 D.注入液氯消毒
(2)已知高铁酸钠(Na2FeO4)加入水中,能杀死水中的微生物和细菌,并能产生类似明矾的净水作用,写出其在净水过程中发生反应的离子方程式____________。(3)刚出厂的自来水中含少量余氯,它在配水管中停留可有效地起到杀菌作用,并能保持较长时间。请解释其原因_______。(4)水中可溶性钙及镁的化合物含量的高低可用水的硬度来表示。下列问题的出现与水的硬度无关的是_____________。A.锅炉管道结垢B.肥皂去污效果降低C.水中溶解氧降低D.长期饮用造成尿道结石
【解析】(1)用碱调节污水到中性的方法不可取,因为这样只是换了一种污染水的方法。(2)Na2FeO4中+6价的铁体现氧化性时变为+3价铁,而Fe3+会水解产生具有净水功能的Fe(OH)3胶体。(3)Cl2与H2O的反应是一个可逆反应,HClO具有杀菌消毒作用,当其被消耗后,由于剩余Cl2的存在,会使Cl2与H2O反应的平衡向生成HClO的方向移动,从而使水中的HClO能得到及时的补充。(4)根据“水中可溶性钙及镁的化合物含量的高低可用水的硬度来表示”的意思,水中溶解氧的降低与水的硬度无关。
答案:(1)B(2)Fe3++3H2O====Fe(OH)3(胶体)+3H+(3)Cl2+H2O HCl+HClO,由于余氯的存在,当次氯酸被消耗后,上述反应的化学平衡向正反应方向移动,使水中的次氯酸得到了及时的补充(答出平衡移动即可)(4)C
3.海洋是人类巨大的化学资源宝库,海洋资源的综合利用具有极为广阔的发展前景。(1)蒸馏法是目前技术和工艺比较成熟的海水淡化方法,但由于使用大量燃煤,造成能耗多,排污量大。针对上述蒸馏法的缺点,请你提出一条改进建议:______________________。
(2)空气吹出法是目前从海水中提取溴的常用方法,流程如图所示(苦卤即海水蒸发结晶分离出食盐后的母液):
①反应Ⅰ后通入“空气、水蒸气”的目的是______________。②反应Ⅲ后先加入四氯化碳,目的是_____________________,从四氯化碳中分离出单质溴的方法是___________________。(3)苦卤中含有NaCl、MgCl2、KCl、MgSO4等盐类物质。用简要的文字说明如何测定苦卤中MgCl2的含量 。
【解析】(1)潮汐能、风能、太阳能等均为绿色能源,可以代替燃煤,降低污染。(2)反应Ⅰ的目的是置换溴,溴被置换出来后溶解在水中,通入热的空气、水蒸气,温度升高,溴被吹出,吹出后的溴与二氧化硫反应,生成Br-,反应Ⅲ是氯气再次氧化Br-,然后用四氯化碳萃取溴,最后通过蒸馏分离出溴。(3)苦卤中有两种镁盐,即硫酸镁和氯化镁。
答案:(1)充分利用潮汐能、风能、太阳能等海边富有的洁净能源(2)①使置换出的溴被吹出来 ②使生成的溴溶解在四氯化碳中(或答“萃取溴”) 蒸馏(3)先用足量BaCl2溶液沉淀 求出 的总量,即求出MgSO4的量,然后用足量NaOH溶液沉淀Mg2+,求出总的Mg2+,减去MgSO4中Mg2+的量即可得到MgCl2的量
4.请回答氯碱工业中的如下问题:(1)氯气、烧碱是电解食盐水时按照二者固定的比率k(质量比)生成的产品。理论上k= (要求写出计算表达式和结果)。(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、S 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是 (填序号)。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 。②分别写出燃料电池B中正极、负极上发生的电极反应。正极: ;负极: 。③这样设计的主要节(电)能之处在于(写出2处)___________。
【解析】(1)根据化学方程式2NaCl+2H2O 2NaOH+H2↑+Cl2↑即可计算出k值。(2)把Na2CO3放在BaCl2之后,以除去过量的Ba2+;把盐酸放在Na2CO3之后,以除去过量的(3)判断出两极是解答电池问题的前提:燃料电池中通空气(氧化剂)的一极应为正极,所以:Y(通入负极,还原剂)必为H2,继而从H2产生于电解池的阴极,可推出产生于电解池阳极的X必为Cl2;a% NaOH溶液进入燃料电池,出来后的浓度变化可用两种方法判断:
[方法一]从Na+的移动方向来定:在燃料电池内部,Na+向正极移动,所以正极处b% NaOH溶液浓度较a% NaOH溶液浓度大,负极流出的NaOH溶液变稀。[方法二]从水、OH-的量变来定:负极2H2-4e-+4OH-====4H2O,水增多、OH-减少,溶液变稀;正极O2+4e-+2H2O====4OH-,水减少、OH-增多,所以正极浓度增大,即a%
人教版 (新课标)选修2 化学与技术第三单元 化学与材料的发展课题2 金属材料课文ppt课件: 这是一份人教版 (新课标)选修2 化学与技术第三单元 化学与材料的发展课题2 金属材料课文ppt课件,共14页。PPT课件主要包含了金属的广泛应用,一从矿石中获得金属,1炼铁,2炼钢,钢铁的冶炼,铝的冶炼,原理和步骤,二金属腐蚀及防止,1化学腐蚀,金属腐蚀等内容,欢迎下载使用。
高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用复习ppt课件: 这是一份高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用复习ppt课件,共20页。PPT课件主要包含了获取纯净的水,海水的综合利用,氯碱工业,汽油C5C11,煤油C11C16,柴油C15C18,重油C20以上,减压蒸馏塔,催化裂化,石油气C4以下等内容,欢迎下载使用。
高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用课文内容ppt课件: 这是一份高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用课文内容ppt课件,共60页。PPT课件主要包含了特别提醒,石油的炼制,煤的综合利用等内容,欢迎下载使用。













