

高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用教案
展开课题2 海水的综合利用
第1课时
教学目标
1.了解氯碱工业反应原理;正确书写电极反应方程式和电解的总化学方程式。
2.初步了解电解槽的简单结构及食盐水的精制。
3.常识性介绍以氯碱工业为基础的化工生产。
4.通过电解食盐水的实验,培养学生的观察能力、分析归纳能力和利用化学原理解决实际问题的能力。
5.通过阅读材料,培养学生的自学能力。
6.通过对实验现象的观察,掌握观察实验的方法和步骤,准确记录实验现象,正确分析实验现象,探究实验规律的方法。通过讨论,激发学生的求知欲,闪现智慧火花,培养创新意识。
教学重点
氯碱工业反应原理。
教学难点
氯碱工业反应原理。
教学方法
演示实验法
教学用具
1.实验仪器:铁架台、U型管、石墨电极、导线、电流表、直流电源。
2.实验药品:饱和氯化钠溶液。
3.幻灯片若干张。
课时安排
2课时
引入新课:
本节课我们学习电解饱和食盐水制烧碱——又称氯碱工业。我们学习的主要目标是掌握工业上制取氯气和烧碱的反应原理,初步了解化工生产设备、原料及其精制、生产流程。
【板书】第二节 氯碱工业
一、电解饱和食盐水反应原理
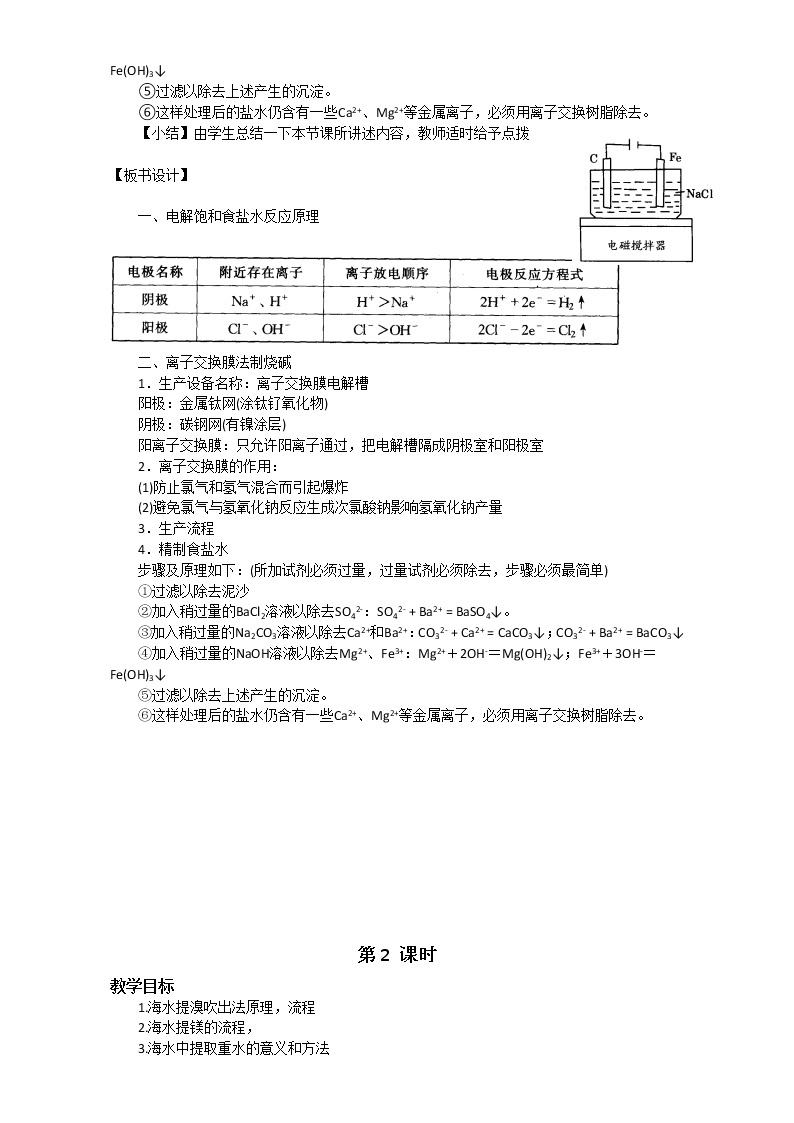
【演示】实验装置如右图:
【投影】实验步骤:
1.按装置图安装好仪器。
2.向U型管中注人饱和食盐水,接通电源。
3.向阴阳两极滴加几滴酚酞溶液,把湿润的淀粉碘化钾试纸分别放在阴阳两极试管口上方。
【设疑】电解池两极上各有什么现象产生?
【提问】请描述实验现象,试判断出结论。
【学生回答】(相互补充)
1.两极均产生气体。
2.阴极区附近溶液出现红色,有碱生成。
3.阳极淀粉碘化钾试纸变蓝,气体有刺激性气味,应是Cl2。
【阅读讨论】阅读教材,看后相互讨论,推选代表回答产生这种现象的原因。
【小结并板书】师生共同总结:
在阴极:由于2H++2e- = H2↑,H+不断被消耗,促进H2O H++OH-向右移动,破坏了水的电离平衡,c (OH-)相对的增大了,因此,在阴极附近形成了氢氧化钠溶液。
【提问】写出电解的总的化学反应方程式。
【板演】2NaCl+2H2O = H2↑+Cl2↑+2NaOH
【追问】这样写是否正确?
【回答】不正确,反应条件应写通电或电解。
【过渡】工业上就是应用电解食盐水溶液的方法制取烧碱和氯气的,下面我们研究工业制碱方法。
【板书】二、离子交换膜法制烧碱
【讲述】目前世界上比较先进的电解制碱技术是离子交换膜法。请同学们结合幻灯片上的自学提纲,阅读教材。
【投影】1.离子交换膜电解槽的简单构造如何?
2.离子交换膜的作用是什么?
3.工业制碱的简单生产流程怎样?
【自学讨论】学生阅读,同学之间可以相互讨论,教师解疑。
【小结】师生共同活动:
【板书】1,生产设备名称:离子交换膜电解槽
阳极:金属钛网(涂钛钌氧化物)
阴极:碳钢网(有镍涂层)
阳离子交换膜:只允许阳离子通过,把电解槽隔成阴极室和阳极室。
2.离子交换膜的作用:
(1)防止氯气和氢气混合而引起爆炸
(2)避免氯气与氢氧化钠反应生成次氯酸钠影响氢氧化钠的产量
3.生产流程(详见教材内容)。
【投影】
【设疑】氯碱工业的原料是饱和食盐水,由于粗盐中含有泥沙、Ca2+、Mg2+、Fe3+、SO42-杂质,会在碱性溶液中形成沉淀,损坏离子交换膜,所以必须要对粗盐水进行净化。那么,如何净化盐水呢?
实际上这是一个物质分离和提纯的问题。请同学们思考:
1.用什么方法除去泥沙?
2.用什么试剂除去Ca2+、Mg2+、Fe3+、SO42-?
3.所用试剂只有过量才能除净这些杂质,你能设计一个合理的顺序逐一除杂吗?
【讨论】同学之间相互讨论探讨。
【归纳总结】师生共同活动。
【板书】4.精制食盐水
步骤及原理如下:(所加试剂必须过量,过量试剂必须除去,步骤必须最简单)
①过滤以除去泥沙。
②加入稍过量的BaCl2溶液以除去SO42-:SO42- + Ba2+ = BaSO4↓。
③加入稍过量的Na2CO3溶液以除去Ca2+和Ba2+:CO32- + Ca2+ = CaCO3↓;CO32- + Ba2+ = BaCO3↓
④加入稍过量的NaOH溶液以除去Mg2+、Fe3+:Mg2++2OH-=Mg(OH)2↓;Fe3++3OH-=Fe(OH)3↓
⑤过滤以除去上述产生的沉淀。
⑥这样处理后的盐水仍含有一些Ca2+、Mg2+等金属离子,必须用离子交换树脂除去。
【小结】由学生总结一下本节课所讲述内容,教师适时给予点拨
【板书设计】
一、电解饱和食盐水反应原理
二、离子交换膜法制烧碱
1.生产设备名称:离子交换膜电解槽
阳极:金属钛网(涂钛钌氧化物)
阴极:碳钢网(有镍涂层)
阳离子交换膜:只允许阳离子通过,把电解槽隔成阴极室和阳极室
2.离子交换膜的作用:
(1)防止氯气和氢气混合而引起爆炸
(2)避免氯气与氢氧化钠反应生成次氯酸钠影响氢氧化钠产量
3.生产流程
4.精制食盐水
步骤及原理如下:(所加试剂必须过量,过量试剂必须除去,步骤必须最简单)
①过滤以除去泥沙
②加入稍过量的BaCl2溶液以除去SO42-:SO42- + Ba2+ = BaSO4↓。
③加入稍过量的Na2CO3溶液以除去Ca2+和Ba2+:CO32- + Ca2+ = CaCO3↓;CO32- + Ba2+ = BaCO3↓
④加入稍过量的NaOH溶液以除去Mg2+、Fe3+:Mg2++2OH-=Mg(OH)2↓;Fe3++3OH-=Fe(OH)3↓
⑤过滤以除去上述产生的沉淀。
⑥这样处理后的盐水仍含有一些Ca2+、Mg2+等金属离子,必须用离子交换树脂除去。
第2 课时
教学目标
1.海水提溴吹出法原理,流程
2.海水提镁的流程,
3.海水中提取重水的意义和方法
教学重点
1.海水提溴吹出法原理,流程
2.海水提镁的流程,
教学方法
展示图片法
教学用具
海水提镁、提溴的图片
课时安排
2课时
教学过程
引入新课:浩瀚的海洋是个巨大的宝库,不仅可以提供给我们丰富的食物、食盐、也是化工生产中重要的资源来源。我们已经知道它是氯碱工业的来源,那么,还有那些行业需要从海洋中获得资源呢?
新课教学:板书:海水提溴
目前,从海洋种提取的溴约占世界溴产量的三分之一。常用的海水提溴的方法叫做吹出法。下面我们看一下它的反应原理
1、氧化
工业上从海水中提取溴时,首先通氯气于pH为3.5左右晒盐后留下苦卤(富含Br-离子)中置换出Br2。
Cl2 +2Br - =Br2+ 2Cl -
2、吹出
然后用空气把Br2吹出,再用Na2C03溶液吸收,即得较浓的NaBr和NaBrO3溶液:
3CO32- + 3Br2 = 5Br- + BrO33- + 3CO2↑
最后,用硫酸将溶液酸化,Br2即从溶液中游离出来:
5Br- + BrO33- + 6H+ = 3Br2 + 3H2O
3、吸收
用还原剂二氧化硫使溴单质变为HBr,再用氯气将其氧化成溴产品。
Br2 + SO2 +2H2O =2HBr+H2SO4
Cl2 +2Br - =Br2+ 2Cl -
工业生产种它的工艺流程有时怎样的呢?
展示图片
不仅可以从海水中提取到溴,还有很多材料,比如说镁
其 反应原理及反应式如下
工业生产流程
除此之外,还可以从海水中提取重水。
氘是氢的同位素。氘的原子核除包含一个质子外,比氢多了一个中子。氘的化学性质与氢一样,但是一个氘原子比一个氢原子重一倍,所以叫做“重氢”。氢二氧一化合成水,重氢和氧化合成的水叫做“重水”。重水主要赋存于海水中,总量可达250亿吨。重水现在已是核反应堆运行不可缺少的辅助材料,也是制取氘的原料
它的制备方法有
蒸馏法:这种方法只能得到纯度为92%的重水;
电解法:可得99.7%的重水,但消耗电能特别大。
高中化学人教版 (新课标)选修2 化学与技术第二单元 化学与资源开发利用课题3 石油、煤和天然气的综合利用教案: 这是一份高中化学人教版 (新课标)选修2 化学与技术第二单元 化学与资源开发利用课题3 石油、煤和天然气的综合利用教案,共3页。教案主要包含了思考与交流等内容,欢迎下载使用。
人教版 (新课标)选修2 化学与技术课题2 表面活性剂 精细化学品教学设计: 这是一份人教版 (新课标)选修2 化学与技术课题2 表面活性剂 精细化学品教学设计,共4页。
高中化学人教版 (新课标)选修2 化学与技术课题1 无机非金属材料教案设计: 这是一份高中化学人教版 (新课标)选修2 化学与技术课题1 无机非金属材料教案设计,共7页。教案主要包含了学情分析,教学目标,教学重难点,学法指导,硅酸盐材料等内容,欢迎下载使用。













