学业水平考试常考考点解题技巧(2022)
展开一、选择题
1、化学键:(1)有金属元素就一定含有离子键;(2)有两种非金属元素(或两种以上)的就有共价键。
2、判断氧化还原反应:有化合价变化的为氧化还原反应(技巧:有单质参加或者生成的反应)
3、氧化剂化合价降低,被还原;还原剂化合价升高,被氧化;
4、原电池: = 1 \* GB3 ①负极失去电子被氧化发生氧化反应(活泼性强的金属做负极,负氧升失氧); = 2 \* GB3 ②化学能转化为电能的装置。
5、原电池:负极:(1)电子流出的一极 (2)失电子的一极(3)发生氧化反应的一极 (4)元素化合价升高的一极 (5)金属活泼性较强的一极
谐音:原电池中浮(负极)只(失去电子)羊(氧化反应)
6、物质的量的计算
×22.4L·ml-1
÷22.4L·ml-1
×cB
÷ cB
÷NA
÷M
物质的量
(n)
×NA
微粒数(N)
质量
(m)
×M
溶液的体积
(V)
气体体积(V)(标准状况)
7、关于:Z质子数(质子数永远等于原子序数,如果是原子或分子,质子数也等于电子数,如果是离子,则质子数不等于电子数);
A质量数(质量数=质子数+中子数;中子数=质量数-质子数)。
8、①常见溶于水放热的物质:CaO(生石灰)、浓硫酸、NaOH(苛性钠、火碱、烧碱);②常见溶于水吸热的物质:NH4NO3(硝酸铵);③常见溶于水不放热也不吸热:NaCl (食盐)。
9、化学变化:铁锅生锈、风化、煤的干馏、煤的气化、石油的裂化、石油的裂解、伐薪烧炭、野火说不尽、蜡炬成灰泪始干(常考燃烧和铁生锈)
物理变化:盐溶于水、酒精挥发、水结成冰、冰雪消融、水落石出、木已成舟、千里冰封、万里雪飘、铁杵磨成针、石油分馏等
10、混合物:碘酒(碘+酒精)、盐酸(HCl+H2O)、红酒白酒啤酒葡萄酒(乙醇+H2O)、食用油、空气、氨水、铁矿石、煤、石油、氯水、石灰水等
纯净物:干冰(CO2)、冰水共存(H2O)、液氯(Cl2)、液氨(NH3)、蔗糖、明矾;
11、电解质和非电解质(化合物):①电解质:酸(例如:H2SO4、CH3COOH)、碱(例如:NaOH)、盐(例如:Na2SO4);非电解质:②非金属氧化物(例如:SO2)、蔗糖、乙醇(C2H5OH);③既不是电解质又不是非电解质:混合物(**溶液)和单质。
12、物质类别
①酸:HCl、H2SO4 、HNO3、CH3COOH;
②碱:KOH、NaOH、Ca(OH)2、Ba(OH)2、NH3。H2O;
③氧化物含有两种元素,其中一种是氧元素: H2O、CO2、CO、NO2、NO、SiO2、P2O5、SO2、SO3、Li2O、Na2O、MgO、Al2O3、CaO、CuO、Fe2O3、Fe3O4、BaO等;
④盐:KCl、NaCl、NH4Cl、BaCl2、CaCl2、CuCl2、MgCl2、AlCl3┄┄
K2CO3、Na2CO3、 (NH4)2CO3、BaCO3、CaCO3、CuCO3、MgCO3┄┄
KHCO3、NaHCO3、NH4HCO3、Ba(HCO3)2、Ca(HCO3)2、Mg(HCO3)2┄┄
K2SO4、Na2SO4、 (NH4)2SO4、BaSO4、CaSO4、CuSO4、MgSO4┄┄
KNO3、NaNO3、NH4NO3、Ba(NO3)2、Ca(NO3)2、Cu(NO3)2、Mg(NO3)2┄┄
K2SiO3、Na2SiO3、 (NH4)2SiO3、BaSiO3、CaSiO3、MgSiO3┄┄
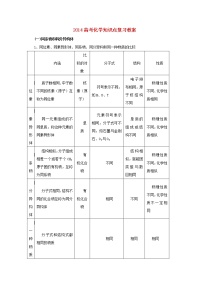
13、几种分散系的比较
14、有机反应类型:①取代反应格式:A+B=C+D (如酯化反应、水解反应)②加成反应格式: A+B=C (产物一般只有一种)③有O2为氧化反应。
15、同位素:质子数相同,中子数不同的原子;例如:、和;和
16、同素异形体:由同种元素组成的不同单质;例如:氧气和臭氧;白磷和红磷;金刚石和石墨;
17、同系物(碳原子数一定不同) :①对象:有机物;②同一类物质(含有相同的官能团);③组成相差1个或若干个CH2。例如:CH4和C3H8;CH3CH2CH2OH和CH3CH2OH。
18、同分异构体(碳原子数一定要相同):分子式相同,结构不同的有机物;
例如:CH3CH2OH和CH3OCH3,葡萄糖与果糖;蔗糖与麦芽糖
注意淀粉与纤维素不互同分异构体
19、常见的高分子化合物有:淀粉、纤维素、蛋白质、聚乙烯(塑料)注意:油脂不是高分子化合物
20、能水解的物质:①纤维素、淀粉葡萄糖 ②油脂高级脂肪酸(钠)+甘油 ,油脂的碱性水解反应称为皂化反应 = 3 \* GB3 ③蛋白质氨基酸
不能水解的物质:葡萄糖、果糖
21、葡萄糖的检验用新制Cu(OH)2或用银氨溶液发生银镜反应。蛋白质的检验:灼烧,可鉴别蚕丝与人造丝 淀粉的检验用碘单质( I2 )
22、金属的活动性顺序:
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb(H)Cu、Hg、Ag、Pt、Au
稀HCl、稀H2SO4 与氢之前的金属反应能放出H2
23、焰色反应是物理变化,是元素的性质。钠元素焰色为黄色,钾元素为紫色(透过蓝色钴玻璃),焰色反应为黄色并不能说不含钾元素。
24、制糕点常用到小苏打:NaHCO₃,纯碱和苏打是Na2CO₃两者溶液显显碱性
两者性质为“三大一小”:溶解性、热稳定性、碱性均为Na2CO₃> NaHCO₃,与盐酸反应的剧烈程度Na2CO₃
26、Na熔点低,密度小,保存在煤油中。Na与水会反应剧烈(浮、熔、游、响、红)
27、铝在空气中能稳定存在的原因是铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化
28、铝既能和酸反应又能和强碱溶液反应放出氢气
29、Al2O3熔点高能作耐火材料,它是刚玉、红宝石、蓝宝石的主要成分,是两性氧化物既能和强酸反应又能和强碱反应
30、Al (OH)3是两性氢氧化物,是两性氢氧化物既能和强酸反应又能和强碱反应
制备Al (OH)3用铝盐和氨水,不用NaOH。
31、明矾的主要成分为KAl(SO4)2∙12H2O,可作净水剂。
32、Fe2O3俗名铁红,是铁锈的主要成分 ;Fe3O4俗名磁性氧化铁
33、检验Fe3+用KSCN溶液,若含Fe3+溶液变红,注意现象为红色溶液,无沉淀
34、除去FeCl3中的FeCl2,加氯水;除去FeCl2中的FeCl3,加铁粉
35、合金是混合物,有熔点低,硬度大的特点。合金有青铜(Cu/Sn)、黄铜(Cu/Zn)、生铁(Fe/C)、钢(Fe/C)、硬铝(Mg/Al)等。
37、
36、卤素之间的置换反应:氧化性:Cl2 >Br2>I2 氧化性强的可置换氧化性弱的Cl2+ 2I-= I2+ 2Cl-
37、NH3能形成喷泉实验因为NH3极易溶于水,NH3溶于水溶液显碱性。
氨气的检验:将湿润的红色石蕊试纸置于试管口,若试纸变蓝则有氨气
铵盐的性质:(1)所有的铵盐都易溶于水 (2)铵盐不稳定,受热易分解
(3)能与强碱反应
38、NO无色有毒气体,难溶于水,易与空气中的氧气反应生成红棕色NO2 ,用排水法收集
铜与稀硝酸反应生成NO,与浓硝酸反应生成NO2 。
即金属与稀硝酸反应生成NO,与浓硝酸反应生成NO2。
39、NO2能与水反应生成硝酸与一氧化氮,用排空气法收集。
40、电子元件、光电池、芯片等主要成分是Si
水晶、石英、石英玻璃、玛瑙、光导纤维、沙子主要成分是SiO2
硅酸H2SiO3 不溶于水,硅胶(主要成分为硅酸)可用于食品干燥剂
Na2SiO3的水溶液叫“水玻璃”常用作耐火材料和黏结剂。
41、玻璃、水泥、陶瓷是三大硅酸盐材料
42、二氧化硅与HF反应用于雕刻玻璃,HF保存在塑料瓶中。
43、SO2和NO2造成酸雨,CO2和CH4造成温室效应,
氟氯代烷(氟利昂)造成臭氧层空洞,氮的氧化物造成光化学烟雾。
44、实验室需要配置一定物质的量浓度用到的玻璃仪器:烧杯、量筒、100mL容量瓶、玻璃棒、胶头滴管;
45、可以加热的仪器:烧杯、试管、圆底烧瓶、蒸发皿、坩埚;
46、关于干燥剂: = 1 \* GB3 ①碱石灰(NaOH+Ca):不能干燥Cl2、HCl 、NO2、、SO2 、CO2等酸性气体; = 2 \* GB3 ②浓硫酸:不能干燥NH3碱性气体; = 3 \* GB3 ③硅胶只能用于干燥食品。
47、两种相互溶解的液体用蒸馏、两种不相溶的物质用分液; = 1 \* GB3 ①能溶于水的有机物有乙酸、乙醇,不能通过分液的方式与水分离,等其他有机物均不溶;
②有机物和有机物是互溶的。
48、 结晶是指从溶液中得到固体溶质的方法;蒸馏指的是把液体加热变成蒸汽,然后冷却又变成液体的方法;
49、粗盐提纯:指的是把含有杂质的氯化钠固体提纯;过程为:溶解→过滤→蒸发结晶;若粗盐提纯中涉及加入某种试剂,则盐酸放在最后加。
50、能用排水法收集的气体:H2、O2、NO、CO、CH4;能用向上排空气法收集的气体:Cl2、CO2、HCl、SO2;能用向下排空气法收集气体:H2、NH3、CH4。
51、该装置表示用固体和液体不加热制备某种气体,收集该气体时,用排水法收集;符合的条件的为:
= 1 \* GB3 ①过氧化氢(H2O2)和MnO2制备氧气O2;
= 2 \* GB3 ②锌粒和稀硫酸制取氢气H2;
= 3 \* GB3 ③铜和稀硝酸制取NO。
52、离子共存: = 1 \* GB3 ①H+只能与NO3-、SO42-、Cl-共存,其他阴离子不可以与之共存;
= 2 \* GB3 ②OH-只能与K+、Na+、Ba+-共存,其他阳离子不可以与之共存;
= 3 \* GB3 ③ Ba+不能与SO42-、CO32-共存;Ca+不能与CO32-共存;Ag+不能与Cl-共存。
53、2Fe + 6H+= 2Fe3++3H2↑是错误的;有色离子:Fe3+、Fe2+、Cu2+、MnO4-。
二、非选择题
1、元素周期表:
◎周期数=电子层数 主族序数=最外层电子数
◎元素周期律:(1)周期表中越右上的元素,非金属性越强;周期表中越左下的元素,金属性越强;(2)非金属性强的元素,氢化物越稳定,最高价氧化物的酸性强;金属性强的元素,最高价氧化物的碱性强;(一强都强原则)
◎原子半径大小比较: = 1 \* GB3 ①电子层越多,半径越大(不同周期原子比较); = 2 \* GB3 ②当电子层相同时,原子序数越大,半径反而越小(序大径小)。
2、有机反应
相关反应如下:
① CH2=CH2 + H2O C2H5OH 加成反应
② 2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
③ 酯化反应或氧化反应
④ 加聚反应
◎甲烷:CH4+Cl2CH3Cl+HCl 取代反应;其中一氯甲烷为气体,二氯甲烷、三氯甲烷和四氯化碳均为液体
◎乙烯:1、六个原子共平面;2、可使溴水或酸性高锰酸钾溶液褪色,用于区分甲烷
◎乙酸(CH3COOH):可以跟碳酸盐、碳酸氢盐反应生成CO2,还能使紫色石蕊试液变红,可以根据此性质来区分乙酸和乙醇。
◎常见物质的结构简式和化学式的对比
3、化学反应原理
◎物质断裂化学键吸热,形成化学键放热
◎放热反应:反应物总能量高于生成物的能量;
◎吸热反应:反应物总能量低于生成物的能量:(1)大多数的分解反应(2)制水煤气C+H2O=CO(g)+H2(g),C+CO2=2CO (3)Ba(OH)2∙8H2O+2NH4Cl=BaCl2+2NH3+10H2O
◎能提高化学反应速率的方法:升温、提高反应物浓度、增大压强、加入适当催化剂、把固体反应碾碎提高表面积。
◎可逆反应达到平衡后(变量不变):①各物质的浓度、物质的量不再改变(定);②正、逆速率相等(等)。
◎速率的计算:△v(A)=△c(A)/△t
◎化学计量数之比等于△c/△n/平均反应速率之比
4、气体制备(Cl2、SO2)
(1)氯气的制备:MnO2 + 4HCl(浓) MnCl2 + Cl2 + 2H2O
Cl2 :黄绿色 有刺激性气味,有毒,密度比空气大 。
Cl2 能使湿润的有色布条褪色原因是Cl2+ H2O =HCl+HClO, HClO具有漂白性。氯水的主要成分:三分子、三离子
Cl2 与碱反应制漂白液的原理是:Cl2+2NaOH=NaCl+NaClO+H2O
Cl2 与碱反应制漂白粉的原理是:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
漂白粉的主要成分CaCl2、Ca(ClO)2 有效成分:Ca(ClO)2
漂白液的主要成分NaCl、NaClO 有效成分:NaClO
SO2的制备:H2SO4(浓) + Na2SO3 = Na2SO4 + SO2↑ + H2O
◎二氧化硫具有漂白性,能使品红溶液褪色,加热颜色重新出现;二氧化硫具有酸性,能使NaOH的酚酞溶液褪色;二氧化硫具有还原性能使酸性高锰酸钾溶液、氯水、溴水褪色。SO2溶于水形成H2SO3
◎浓硫酸具有吸水性、脱水性和强氧化性 ,碳化属于脱水性。
◎常温下浓H2SO4、浓HNO3 遇到铁、铝会钝化,所以常温下可以铝制或铁制容器来盛放浓H2SO4、浓HNO3 注意:钝化是化学反应,在金属表面形成致密氧化膜。浓硫酸三大特性:①吸水性:浓硫酸用作干燥剂 ②脱水性:用玻璃棒蘸取浓硫酸在滤纸上、滤纸变黑 ③强氧化性
◎SO42-的检验:先加盐酸(HCl)酸化,再加氯化钡(BaCl2);
◎Cl-的检验:先加硝酸(HNO3)酸化,再加硝酸银(AgNO3)溶液;现象:都是能产生白色沉淀。
分散系
分散质粒子直径大小
是否有丁达尔效应
稳定性
举例
浊液
大于100nm
无
不稳定
泥水
溶液
小于1nm
无
稳定
NaCl溶液
胶体
1~100nm
有
介稳定
Fe(OH)3胶体
周期数
ⅠA
ⅡA
ⅢA
ⅠVA
VA
VⅠA
ⅡVA
稀有气体
1
H
He
2
Li
Be
B
C
N
O
F
Ne
3
Na
Mg
Al
Si
P
S
Cl
Ar
4
K
Ca
Br
最外层电子数
1
2
3
4
5
6
7
8
物质
甲烷
乙烯
苯
乙醇
乙酸
结构
简式
CH4
CH2=CH2
CH3CH2OH
CH3COOH
分子式
CH4
C2H4
C6H6
C2H6O
C2H4O2
性质
稳定
氧化、加聚
氧化、酯化
酸性、酯化
2022高考化学一轮复习教案:专题突破(八) 突破酸碱中和图像中的五个关键点: 这是一份2022高考化学一轮复习教案:专题突破(八) 突破酸碱中和图像中的五个关键点,共16页。
高考化学知识点复习教案20: 这是一份高考化学知识点复习教案20,共9页。
高考化学知识点复习教案9: 这是一份高考化学知识点复习教案9,共4页。教案主要包含了领悟·整合,联想·发散,知识·链接,启发·引申,专题放送等内容,欢迎下载使用。