



高考化学真题分项汇编(全国通用)五年(2019-2023)专题10+水溶液中的离子反应与平衡
展开五年(2019-2023)年高考真题分项汇编
专题10 水溶液中的离子反应与平衡
〖2023年高考真题〗
考点一 电离平衡
1.(2023·浙江卷)草酸()是二元弱酸。某小组做如下两组实验:
实验I:往溶液中滴加溶液。
实验Ⅱ:往溶液中滴加溶液。
[已知:的电离常数,溶液混合后体积变化忽略不计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中时,溶液中
考点二 盐类的水解
2.(2023·北京卷)下列过程与水解反应无关的是
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和溶液制备胶体
考点三 沉淀溶解平衡
3.(2023·全国甲卷)下图为和在水中达沉淀溶解平衡时的关系图(;可认为离子沉淀完全)。下列叙述正确的是
A.由点可求得
B.时的溶解度为
C.浓度均为的和可通过分步沉淀进行分离
D.混合溶液中时二者不会同时沉淀
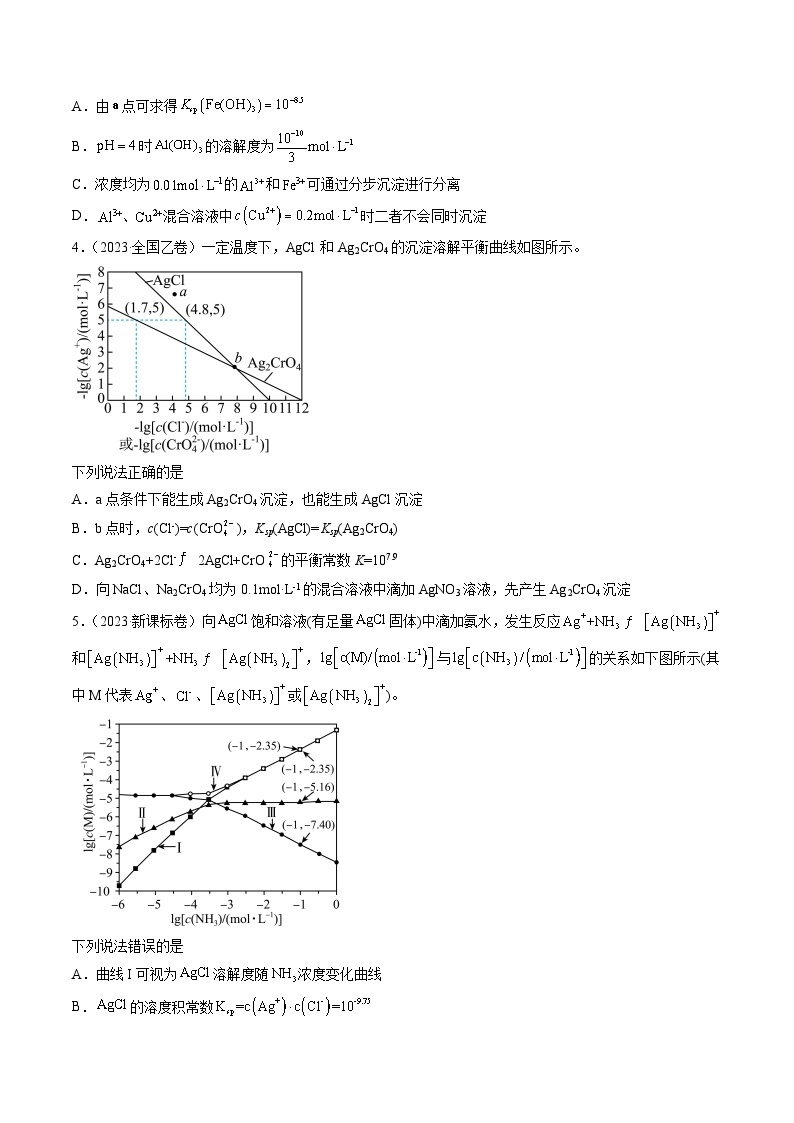
4.(2023·全国乙卷)一定温度下,AgCl和Ag2CrO4的沉淀溶解平衡曲线如图所示。
下列说法正确的是
A.a点条件下能生成Ag2CrO4沉淀,也能生成AgCl沉淀
B.b点时,c(Cl-)=c(CrO),Ksp(AgCl)=Ksp(Ag2CrO4)
C.Ag2CrO4+2Cl-2AgCl+CrO的平衡常数K=107.9
D.向NaCl、Na2CrO4均为0.1mol·L-1的混合溶液中滴加AgNO3溶液,先产生Ag2CrO4沉淀
5.(2023·新课标卷)向饱和溶液(有足量固体)中滴加氨水,发生反应和,与的关系如下图所示(其中M代表、、或)。
下列说法错误的是
A.曲线I可视为溶解度随浓度变化曲线
B.的溶度积常数
C.反应的平衡常数K的值为
D.时,溶液中
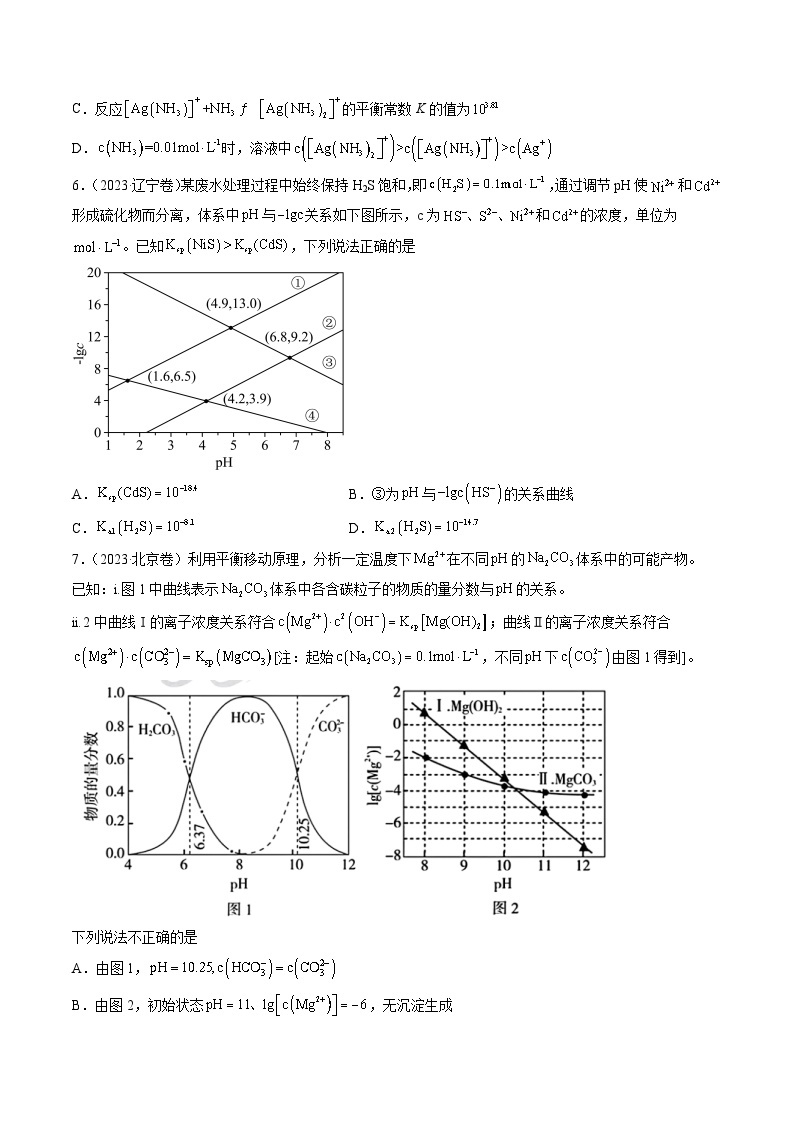
6.(2023·辽宁卷)某废水处理过程中始终保持H2S饱和,即,通过调节pH使和形成硫化物而分离,体系中与关系如下图所示,c为和的浓度,单位为。已知,下列说法正确的是
A. B.③为与的关系曲线
C. D.
7.(2023·北京卷)利用平衡移动原理,分析一定温度下在不同的体系中的可能产物。
已知:i.图1中曲线表示体系中各含碳粒子的物质的量分数与的关系。
ii.2中曲线Ⅰ的离子浓度关系符合;曲线Ⅱ的离子浓度关系符合[注:起始,不同下由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态,无沉淀生成
C.由图2,初始状态,平衡后溶液中存在
D.由图1和图2,初始状态、,发生反应:
考点四 电解质溶液图像分析
8.(2023·山东卷)在含HgI2(g)的溶液中,一定c(I-)范围内,存在平衡关系:;;;;,平衡常数依次为。已知、,、随的变化关系如图所示,下列说法错误的是
A.线表示的变化情况 B.随增大,先增大后减小
C. D.溶液中I元素与元素的物质的量之比始终为
9.(2023·湖北卷)为某邻苯二酚类配体,其,。常温下构建溶液体系,其中,。体系中含Fe物种的组分分布系数δ与pH的关系如图所示,分布系数,已知,。下列说法正确的是
A.当时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C.的平衡常数的lgK约为14
D.当时,参与配位的
10.(2023·湖南卷)常温下,用浓度为的标准溶液滴定浓度均为的和的混合溶液,滴定过程中溶液的随()的变化曲线如图所示。下列说法错误的是
A.约为
B.点a:
C.点b:
D.水的电离程度:
〖2022年高考真题〗
考点一 电离平衡
11.(2022·全国乙卷)常温下,一元酸的。在某体系中,与离子不能穿过隔膜,未电离的可自由穿过该膜(如图所示)。
设溶液中,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度为
C.溶液Ⅰ和Ⅱ中的不相等
D.溶液Ⅰ和Ⅱ中的之比为
12.(2022·福建卷)探究醋酸浓度与电离度关系的步骤如下,与相关步骤对应的操作或叙述正确的
步骤
操作或叙述
A
Ⅰ.用标准溶液标定醋酸溶液浓度
滴定时应始终注视滴定管中的液面
B
Ⅱ.用标定后的溶液配制不同浓度的醋酸溶液
应使用干燥的容量瓶
C
Ⅲ.测定步骤Ⅱ中所得溶液的
应在相同温度下测定
D
Ⅳ.计算不同浓度溶液中醋酸的电离度
计算式为
考点二 水的电离与pH计算
13.(2022·浙江卷)时,向浓度均为的盐酸和醋酸的混合溶液中逐滴加入的溶液(酷酸的;用的溶液滴定等浓度的盐酸,滴定终点的突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加溶液至的过程中,发生反应的离子方程式为:
C.滴定过程中,
D.时,
考点三 盐类的水解
14.(2022·北京卷)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
15.(2022·海南卷)NaClO溶液具有添白能力,已知25℃时,。下列关于NaClO溶液说法正确的是
A.0.01mol/L溶液中,
B.长期露置在空气中,释放,漂白能力减弱
C.通入过量,反应的离子方程式为
D.25℃,的NaClO和HClO的混合溶液中,
16.(2022·浙江卷)时,苯酚的,下列说法正确的是
A.相同温度下,等的和溶液中,
B.将浓度均为的和溶液加热,两种溶液的均变大
C.时,溶液与溶液混合,测得,则此时溶液中
D.时,的溶液中加少量固体,水的电离程度变小
17.(2022·江苏卷)一种捕集烟气中CO2的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO2,若通入CO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含碳物种的浓度c总=c(H2CO3)+c()+c()。H2CO3电离常数分别为Ka1=4.4×10-7、Ka2=4.4×10-11。下列说法正确的是
A.KOH吸收CO2所得到的溶液中:c(H2CO3)>c()
B.KOH完全转化为K2CO3时,溶液中:c(OH-)= c(H+)+c()+c(H2CO3)
C.KOH溶液吸收CO2,c总=0.1mol∙L-1溶液中:c(H2CO3)>c()
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
考点四 沉淀溶解平衡
18.(2022·湖南卷)室温时,用的标准溶液滴定浓度相等的、和混合溶液,通过电位滴定法获得与的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于时,认为该离子沉淀完全。,,)。下列说法正确的是
A.a点:有白色沉淀生成
B.原溶液中的浓度为
C.当沉淀完全时,已经有部分沉淀
D.b点:
19.(2022·福建卷)锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有和杂质离子,可在0~14范围内调节对其净化(即相关离子浓度)。时,与关系见下图(碱性过强时和会部分溶解)。下列说法正确的是
A.可被净化的区间最大
B.加入适量,可进一步提升净化程度
C.净化的先后顺序:
D.
20.(2022·海南卷)某元素M的氢氧化物在水中的溶解反应为:、,25℃,-lgc与pH的关系如图所示,c为或浓度的值,下列说法错误的是
A.曲线①代表与pH的关系
B.的约为
C.向的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以存在pH=9.0,体系中元素M主要以存在
D.向的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以存在
考点五 电解质溶液图像分析
21.(2022·山东卷)工业上以为原料生产,对其工艺条件进行研究。现有含的、溶液,含的、溶液。在一定pH范围内,四种溶液中随pH的变化关系如图所示。下列说法错误的是
A.反应的平衡常数
B.
C.曲线④代表含的溶液的变化曲线
D.对含且和初始浓度均为的混合溶液,时才发生沉淀转化
22.(2022·辽宁卷)甘氨酸是人体必需氨基酸之一、在时,、和的分布分数【如】与溶液关系如图。下列说法错误的是
A.甘氨酸具有两性
B.曲线c代表
C.的平衡常数
D.
〖2021年高考真题〗
考点一 电离平衡
23.(2021·浙江)某同学拟用计测定溶液以探究某酸HR是否为弱电解质。下列说法正确的是
A.25℃时,若测得溶液,则HR是弱酸
B.25℃时,若测得溶液且,则HR是弱酸
C.25℃时,若测得HR溶液,取该溶液,加蒸馏水稀释至,测得,则HR是弱酸
D.25℃时,若测得NaR溶液,取该溶液,升温至50℃,测得,,则HR是弱酸
考点二 电解质溶液图像分析
24.(2021·全国乙)HA是一元弱酸,难溶盐MA的饱和溶液中随c(H+)而变化,不发生水解。实验发现,时为线性关系,如下图中实线所示。
下列叙述错误的是
A.溶液时,
B.MA的溶度积度积
C.溶液时,
D.HA的电离常数
25.(2021·浙江)取两份 的溶液,一份滴加的盐酸,另一份滴加溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是
A.由a点可知:溶液中的水解程度大于电离程度
B.过程中:逐渐减小
C.过程中:
D.令c点的,e点的,则
26.(2021·湖南)常温下,用的盐酸分别滴定20.00mL浓度均为三种一元弱酸的钠盐溶液,滴定曲线如图所示。下列判断错误的是
A.该溶液中:
B.三种一元弱酸的电离常数:
C.当时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
27.(2021·山东)赖氨酸[H3N+(CH2)4CH(NH2)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H3RCl2)在水溶液中存在如下平衡:H3R2+H2R+HRR-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=,下列表述正确的是
A.>
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H2R+)+c(Na+)+c(H+)
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
〖2020年高考真题〗
考点一 水的电离与pH计算
28.(2020·浙江卷)下列说法不正确的是( )
A. 的盐酸中
B. 将KCl溶液从常温加热至80℃,溶液的pH变小但仍保持中性
C. 常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D. 常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
29.(2020·浙江卷)常温下,用氨水滴定浓度均为的和的混合液,下列说法不正确的是( )
A. 在氨水滴定前,和的混合液中
B. 当滴入氨水时,
C. 当滴入氨水时,
D. 当溶液呈中性时,氨水滴入量大于,
考点二 盐类的水解
30.(2020·天津卷)常温下,下列有关电解质溶液的说法错误的是
A. 相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则
B. 相同浓度的CH3COOH和CH3COONa两溶液等体积混合后pH约为4.7,则溶液中
C. FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
D. 在溶液中,
31.(2020·江苏卷)室温下,将两种浓度均为的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
A. 混合溶液(pH=10.30):
B. 氨水-NH4Cl混合溶液(pH=9.25):
C. 混合溶液(pH=4.76):
D. 混合溶液(pH=1.68,H2C2O4为二元弱酸):
考点三 电解质溶液图像分析
32.(2020·新课标Ⅰ)以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:]
下列叙述正确的是
A. 曲线①代表,曲线②代表
B. H2A溶液的浓度为0.2000 mol·L−1
C. HA−的电离常数Ka=1.0×10−2
D. 滴定终点时,溶液中
33.(2020·山东卷)25℃时,某混合溶液中,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是
A. O点时,
B. N点时,
C. 该体系中,
D. pH由7到14的变化过程中, CH3COO-的水解程度始终增大
〖2019年高考真题〗
考点一 电离平衡
34.[2019新课标Ⅲ]设NA为阿伏加德罗常数值。关于常温下pH=2的H3PO4溶液,下列说法正确的是
A.每升溶液中的H+数目为0.02NA
B.c(H+)= c()+2c()+3c()+ c(OH−)
C.加水稀释使电离度增大,溶液pH减小
D.加入NaH2PO4固体,溶液酸性增强
考点二 盐类的水解
35.[2019江苏]室温下,反应+H2OH2CO3+OH−的平衡常数K=2.2×10−8。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.2 mol·L−1氨水:c (NH3·H2O)>c()> c (OH−)> c (H+)
B.0.2 mol·L−1NH4HCO3溶液(pH>7):c ()> c ()> c (H2CO3)> c (NH3·H2O)
C.0.2 mol·L−1氨水和0.2 mol·L−1NH4HCO3溶液等体积混合:c()+c(NH3·H2O)=c(H2CO3)+c ()+
c()
D.0.6 mol·L−1氨水和0.2 mol·L−1 NH4HCO3溶液等体积混合:c (NH3·H2O)+ c()+ c(OH−)=
0.3 mol·L−1+ c (H2CO3)+ c (H+)
考点三 沉淀溶解平衡
36.[2019新课标Ⅱ]绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
A.图中a和b分别为T1、T2温度下CdS在水中的溶解度
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
考点四 电解质溶液图像分析
37.[2019新课标Ⅰ]NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10−3 ,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2−的导电能力之和大于HA−的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)
38.[2019北京]实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CH3COONa溶液的c(OH−)减小
C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
39.[2019天津]某温度下,和的电离常数分别为和。将和体积均相同的两种酸溶液分别稀释,其随加水体积的变化如图所示。下列叙述正确的是
A.曲线Ⅰ代表溶液
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中、分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与恰好中和后,溶液中相同
高考化学真题分项汇编(全国通用)五年(2019-2023)专题14+化学实验综合题: 这是一份高考化学真题分项汇编(全国通用)五年(2019-2023)专题14+化学实验综合题,文件包含高考化学真题分项汇编全国通用五年2019-2023专题14化学实验综合题解析版docx、高考化学真题分项汇编全国通用五年2019-2023专题14化学实验综合题原卷版docx等2份试卷配套教学资源,其中试卷共104页, 欢迎下载使用。
高考化学真题分项汇编(全国通用)五年(2019-2023)专题11+化学实验基础: 这是一份高考化学真题分项汇编(全国通用)五年(2019-2023)专题11+化学实验基础,文件包含高考化学真题分项汇编全国通用五年2019-2023专题11化学实验基础解析版docx、高考化学真题分项汇编全国通用五年2019-2023专题11化学实验基础原卷版docx等2份试卷配套教学资源,其中试卷共54页, 欢迎下载使用。
高考化学真题分项汇编(全国通用)五年(2019-2023)专题09+化学反应速率与化学平衡: 这是一份高考化学真题分项汇编(全国通用)五年(2019-2023)专题09+化学反应速率与化学平衡,文件包含高考化学真题分项汇编全国通用五年2019-2023专题09化学反应速率与化学平衡解析版docx、高考化学真题分项汇编全国通用五年2019-2023专题09化学反应速率与化学平衡原卷版docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。












