化学选修5 有机化学基础第二章 烃和卤代烃综合与测试导学案及答案
展开1、了解烷烃、烯烃、炔烃的物理性质的变化与分子中碳原子数目的关系;
2、能以典型代表物为例,理解烷烃、烯烃、炔烃和卤代烃等有机化合物的化学性质;
3、能根据有机化学反应原理,初步学习实验方案的设计、评价、优选并完成实验;
4、在实践活动中,体会有机化合物在日常生活中的重要应用,同时关注有机物的合理使用。
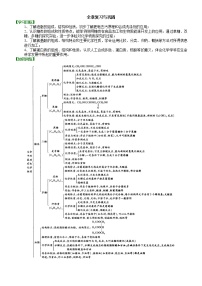
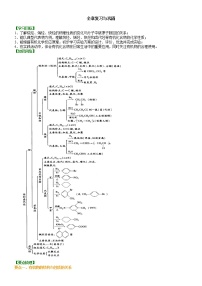
【知识网络】
【要点梳理】
要点一、有机物的结构与性质的关系
1、有机物结构对物理性质的影响。
①组成与结构相似的物质,相对分子质量越大,熔、沸点越高。相对分子质量相近或相同时,支链越多,熔点越低;在不考虑对称结构的分子式前提下,沸点也越低(结构对称的化合物的沸点一般比相同相对分子质量的化合物高)。
②组成与结构不相似的物质,当相对分子质量相近或相同时,分子的极性越大,熔、沸点越高。
③有机物一般不溶于水,而易溶于有机溶剂。但当有机物分子的极性较大时,则可溶于水,如乙醇、乙醛、乙酸等均可溶于水。
2、有机物的结构对化学性质的影响。
①有机物的性质由其分子结构决定,而官能团是决定有机物化学性质的主要因素,一般地,具有相同官能团的有机物具有相似的化学性质,有机物含有多个官能团时,也应具有多个官能团的性质。
②分子作为一个整体,组成的各原子或原子团之间存在着相互影响。尤其是相邻的原子或原子团之间的影响较大。如中,由于苯环对羟基(—OH)的影响,使得的—OH更活泼,表现出弱酸性;由于—OH对苯环的影响,使得的苯环上2,4,6位的氢原子更活泼,室温下就能与浓溴水发生取代反应,生成(三溴苯酚)白色沉淀。
要点二、乙烷、乙烯、乙炔的结构和性质的比较
各类烃与液溴、溴水、酸性KMnO4溶液反应的比较
要点三、重要的有机化学反应
熟练掌握本章中所学的取代、加成、消去、氧化和加聚等反应,包括反应条件、反应类型、方程式的书写、反应条件的选择等,尤其是单体与加聚产物的相互推导,由以前的定性推断发展为定量计算,更应引起重视。
常见的烃的相互转化关系图。
要点四、烃类的重要规律及其应用。
1、等量的烃完全燃烧时耗氧量的计算。
①等物质的量的烃完全燃烧时耗氧量的计算。
对于等物质的量(1 m1)的烃CxHy完全燃烧时,消耗氧气的物质的量为ml,若的值越大,消耗氧气的物质的量也越大。
②等质量的烃完全燃烧时耗氧量的计算。
等质量的烃CxHy完全燃烧时,若烃分子中氢元素的质量分数越大,其耗氧量也越大。即若的值越大。则该烃完全燃烧时的耗氧量也越大。
2、烃分子含氢原子数恒为偶数,其相对分子质量恒为偶数。
应用:如果你求得的烃分子(烃基除外)所含H原子数为奇数或相对分子质量为奇数,则求算一定有错。
请想一想:有机物CxHyOa、CxHyXa(X代表F、Cl、Br、I等卤素),其分子内的氢原子数、相对分子质量是奇数还是偶数?
3、烃燃烧反应中烃前配平化学计量数的变化规律。
设m、n、p、q为正整数,对mCxHy+nO2pCO2+qH2O(设已配平),其中烃前配平化学计量数只有两种可能:非l即2。①当y/2=偶数时,则m=1;②当y/2=奇数时,则m=2。
如:配平C6H6和C3H8分别完全燃烧反应的方程式。
因6/2=3(奇数),烃前配平化学计量数为2;因8/2=4(偶数),烃前配平化学计量数为1,可速得:
2C6H6+15O212CO2+6H2O
C3H8+5O23CO2+4H2O
4、燃烧前后气体体积大小变化规律。
对mCxHy+nO2pCO2+qH2O,若水为气体,则:
当y=4时,反应前后体积相等;
当y>4时,反应后气体体积>反应前气体体积:
当y<4时,反应后气体体积<反应前气体体积。
燃烧前后体积的变化只与H原子数有关。
5、烃类混合物燃烧的耗氧量规律。
①最简式相同的有机物,无论以何种比例混合。只要混合物的质量一定,完全燃烧后生成的CO2、H2O的量为定值,耗氧量也为定值。
②混合物总质量一定,只要含碳(或氢)的质量分数一定,生成CO2(或H2O)的量就相同,但耗氧量可能不同。
【典型例题】
类型一、烃的燃烧及有关计算
例1 现有CH4、C2H4、C2H4、C3H6、C3H8五种有机物,同质量的以上物质中,在相同状况下体积最大的是________;同质量的以上物质完全燃烧时耗O2的量最多的是________;同状况、同体积的以上物质完全燃烧时耗O2的量最多的是________;同质量的以上物质完全燃烧时,生成的CO2最多的是________,生成的水最多的是________。在120℃,1.01×105 Pa时,以上气态烃和足量的O2点燃完全燃烧,相同条件下测得反应前后气体体积没有发生变化的是________。
【思路点拨】等质量的五种气体,摩尔质量越大则气体的物质的量越大,在相同状况下体积也越大;分析烃燃烧的通式,可得出耗氧情况。
【答案】CH4 CH4 C3H8 C2H4、C3H6 CH4 CH4、C2H4
【解析】(1)同质量的以上烃完全燃烧,体积大小取决于气体的物质的量,所以应选CH4,当的值越大,耗氧量越多,生成的H2O的物质的量越大,CO2的物质的量越少。
(2)相同条件下,同体积、同物质的量的烃完全燃烧,耗氧量取决于的相对大小,当水为气态时,y=4,燃烧前后体积不变。
【总结升华】本题重点考查了烃的燃烧规律和计算,是本章的重点,同时也是高考的热点,解题关键是熟练掌握方程式的不同写法和燃烧规律。
举一反三:
【变式1】某气态烃在密闭容器中与氧气混合完全燃烧,若燃烧前后容器压强保持不变(120℃),则此气态烃是( )
A.C2H6 B.C2H4
C.C2H2 D.C3H8
【答案】B
类型二、烃和卤代烃的结构及性质
例2 有机物的结构式中,四价的碳原子以1个、2个、3个或4个单键分别在连接1、2、3和4个其他碳原子时,被分别称为伯、仲、叔或季碳原子,例如化合物A中有5个伯碳原子,仲、叔、季碳原子各1个。
请回答以下问题:
(1)化合物A是汽油燃烧品质和抗震性能的参照物,它的系统名称是________,它的沸点比正辛烷的________(填写下列选项的字母);
A.高 B.低 C.相等 D.不能肯定
(2)用5个叔碳原子和5个伯碳原子(其余为氢原子)构造饱和烃的结构可能有________种,请写出它们的结构简式________;
(3)只由8个叔碳原子(其余为氢原子)构造一个不含双键、三键的结构简式为________。
【思路点拨】相同碳数的烃,支链越多,沸点越低。注意准确分析利用题给信息。
【答案】(1)2,2,4-三甲基戊烷 B
【解析】本题属于有机结构题。考查的知识点有:(1)有机物的命名;(2)同分异构体的书写;(3)有机物熔、沸点高低的一般规律。
对有机物A的命名,首先由结构简式判断其类型,然后由有机物命名规则进行命名。
有机物A与正辛烷都是饱和链烃,它们的熔、沸点的相对大小.可由同类物质熔、沸点高低比较的一般规律得出。
由5个叔碳原子和5个伯碳原子构造饱和烃的结构时,应先由烃分子的碳原子个数5+5=10和氢原子数5×3+5×1=20,求出烃的分子式为C10H20,判断其为环烷烃,分子结构中必含有碳环,写它的同分异构体时,应先写出一个含最大环的环烷烃,此环烷烃含有5个仲碳原子,若再各连上一个伯碳原子正好满足题目要求。然后只需依次逐一缩小碳环,并根据取代基的数目、种类及相对位置写出所有的同分异构体即可。
由8个叔碳原子构造不舍双键、三键的有机物时,可先求出该烃的分子式为C8H8,因不合C≡C键和C=C键,所以必须是每个叔碳原子跟另外其他3个叔碳原子相连接,成为立体结构的烃,才符合题目要求。
【总结升华】本题属于信息题,考查学生接收新信息的能力。建议在学习过程中从不同角度分类整理、对比记忆,会使有机化学的知识树更牢固,并且解题速度也会相应有大幅提高。
举一反三:
【变式1】下列有机分子中,所有的原子不可能处于同一平面的是( )
A、CH2=CH-CN B、CH2=CH-CH=CH2
C、 D、
【答案】D
【解析】A项,所有原子一定处于同一平面;B项所有原子可能处于同一平面,注意中间的碳碳单键可以旋转;C项所有原子可能处于同一平面,苯环与乙烯基间的单键可以旋转;D项可通过甲基判断不可能在同一平面。
类型三、有机实验
例3 实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10% NaOH 溶液洗;⑤水洗。正确的操作顺序是( )
A、①②③④⑤ B、②④⑤③① C、④②③①⑤ D、②④①⑤③
【思路点拨】本题考查粗溴苯的提纯,粗溴苯中主要含有溴、苯、溴化铁等杂质。
【答案】B
【解析】先用水洗,FeBr3溶于水而被洗去;再用NaOH溶液洗,溴与NaOH溶液反应生成易溶于水的盐(NaBr和NaBrO)而被洗去;第二次用水洗时有效地除去残存在有机物中易溶于水的杂质;干燥时少量的水被除去,最后蒸馏时将溴苯中的苯分离出去(利用两者沸点的差异)。
【总结升华】首先应该知道被提纯物质中所含的杂质是什么。除杂质的方法有很多,可应用在不同溶剂中的溶解性的差异、物质的沸点差异等。
举一反三:
【变式1】化学工作者从有机反应RH+Cl2(气)→RCl(液)+HCl(气)受到启发,提出在农药和有机合成工业中可以获得副产品盐酸的设想已成为现实。试指出从上述反应产物中分离得到盐酸的最佳方法是 ( )
A、蒸馏法 B、水洗分液法 C、升华法 D、有机溶剂萃取法
【答案】B结构、性质
乙烷
乙烯
乙炔
结构简式
CH3—CH3
CH2=CH2
CH≡CH
结构特点
全部为单键;饱和链烃;正四面体型结构
含碳碳双键;不饱和链烃;平面型分子,键角120°
含碳碳三键;不饱和链烃;直线型分子,键角180°
物理性质
无色气体,难溶于水而易溶于有机溶剂,密度比水小
——
——
化
学
性
质
化学活动性
稳定
活泼
活泼
取代反应
光卤代
——
——
加成反应
——
能与H2、X2、HX、H2O、HCN等发生加成反应
氧化反应
燃烧火焰较明亮
燃烧火焰明亮,带黑烟
燃烧火焰很明亮,带浓黑烟
不与酸性KMnO4溶液反应
使酸性KMnO4溶液褪色
使酸性KMnO4溶液褪色
加聚反应
不能反应
能反应
能反应
鉴别
不能使溴水褪色;不能使酸性KMnO4溶液褪色
能使溴水褪色;能使酸性KMnO4溶液褪色
物质类别
液溴
溴水
酸性KMnO4溶液
烷烃
光照条件下取代
不反应,液态烷烃可将溴萃取褪色
不反应
烯烃
加成
加成褪色
氧化褪色
炔烃
加成
加成褪色
氧化褪色
苯
一般不反应,催化下可取代
不反应,苯可将溴萃取褪色
不反应
苯的同系物
一般不反应,催化下可取代
不反应,苯的同系物可将溴萃取褪色
氧化褪色
反应类型
定义
举例(反应的化学方程式)
取代反应
有机物分子里的原子或原子团被其他原子或原子团所代替的反应
加成反应
有机物分子中不饱和原子之间的部分化学键断开,不饱和原子与其他原子或原子团直接结合生成新的化合物的反应
CH2=CH2+Br2—→CH2Br—CH2Br
聚合反应
由相对分子质量较小的化合物分子相互结合成相对分子质量较大的高分子的反应。聚合反应包括加聚反应和缩聚反应
消去反应
有机物在一定条件下,从一个分子中脱去一个小分子(如H2O、HBr等),而生成不饱和(含双键或三键)化合物的反应
CH3CH2OHCH2=CH2↑+H2O
CH3—CH2Br+NaOHCH2=CH2↑+NaBr+H2O
氧化反应
有机物得氧或失氢的反应
2CH3CH2OH+O22CH3CHO+2H2O
2CH3CHO+O22CH3COOH
高中化学第五章 进入合成高分子化合物的时代综合与测试导学案: 这是一份高中化学第五章 进入合成高分子化合物的时代综合与测试导学案,共6页。学案主要包含了学习目标,知识网络,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。
高中化学第五章 进入合成高分子化合物的时代综合与测试导学案: 这是一份高中化学第五章 进入合成高分子化合物的时代综合与测试导学案,共6页。学案主要包含了学习目标,知识网络,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。
人教版 (新课标)选修5 有机化学基础第四章 生命中的基础有机化学物质综合与测试学案及答案: 这是一份人教版 (新课标)选修5 有机化学基础第四章 生命中的基础有机化学物质综合与测试学案及答案,共6页。学案主要包含了学习目标,知识网络,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。