




初中鲁教版第一节 酸及其性质教学课件ppt
展开第1课时 常见的酸及其化学性质
第七单元 常见的酸和碱
第一节 酸及其性质
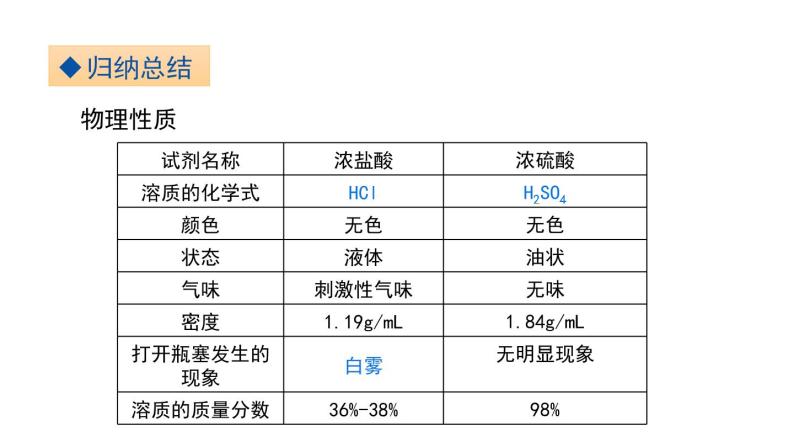
打开瓶塞,观察发生的现象;闻一闻是否有气味?浓盐酸、浓硫酸具有怎样的颜色、状态、气味?
点击图片播放盐酸硫酸视频
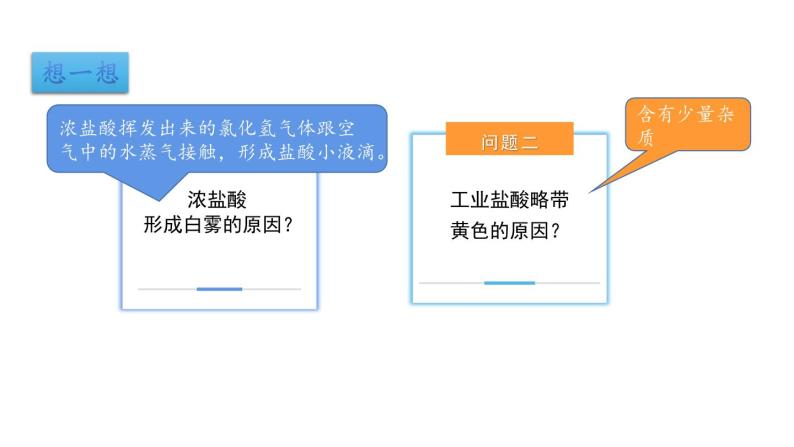
浓盐酸 形成白雾的原因?
工业盐酸略带黄色的原因?
浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气接触,形成盐酸小液滴。
闻气体的气味需要注意什么?
闻气体的气味时不可凑近瓶口,要小心地打开瓶塞,用手在瓶口处轻轻扇动,仅使极少量的气体飘进鼻孔。
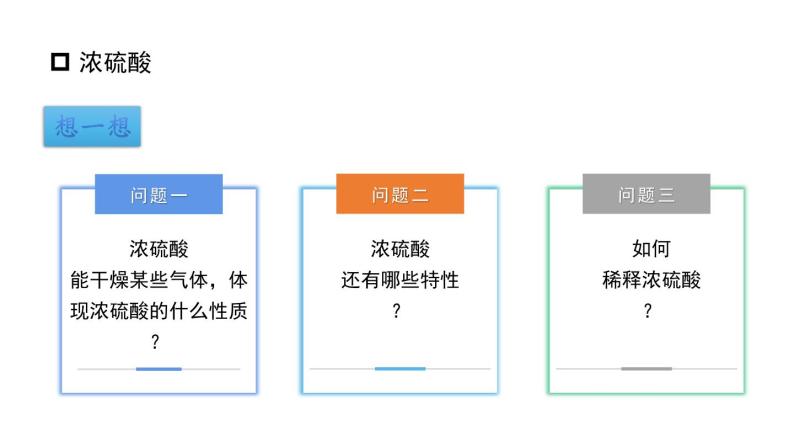
浓硫酸能干燥某些气体,体现浓硫酸的什么性质?
浓硫酸稀释的错误操作
浓硫酸有很强的吸水性可以利用浓硫酸的吸水性将其作为干燥剂。
浓硫酸具有很强的腐蚀性浓硫酸滴到纸张、蔗糖上,会使纸张、蔗糖炭化。稀硫酸滴到纸张上,在水分挥发的过程中使纸张逐渐炭化。浓硫酸还会腐蚀衣物和皮肤。
浓硫酸的稀释溶于水放出大量的热量,将浓硫酸沿着容器内壁慢慢注入水中,并用玻璃棒不断搅拌。切不可将水倒入浓硫酸中,否则可能导致硫酸液滴向四周飞溅。
【例1】下列关于浓盐酸的叙述正确的是( ) A.浓盐酸是一种无色无味的液体 B.浓盐酸在空气中会冒白烟 C.浓盐酸敞口放置一段时间后,溶质质量和溶质质量分数都会减小 D.盐酸就是液态氯化氢
【例2】下列关于浓硫酸的性质叙述不正确的是( ) A.浓硫酸有吸水性,常用作干燥剂 B.浓硫酸能使蔗糖炭化,说明浓硫酸具有吸水性 C.用玻璃棒蘸取浓硫酸在白纸上写字,白纸逐渐变黄,最后变黑 D.浓硫酸“伤熊”事件,说明浓硫酸有强腐蚀性
夺取含有碳、氢、氧等元素的化合物组成里的水分
1.下列有关浓盐酸的叙述正确的是( )A.浓盐酸是一种无色无味的液体 B.打开盛浓盐酸的试剂瓶的瓶塞,瓶口有白烟产生C.浓盐酸中的溶质是HCl ,能使紫色石蕊溶液变蓝D.浓盐酸敞口放置一段时间后,溶液质量会减小
2.下列关于溶质质量分数为98%的浓硫酸的性质说法错误的是( )A.浓硫酸的密度大于水的密度B.浓硫酸与水混合时溶液温度迅速升高C.浓硫酸具有很强的吸水性,可作干燥剂D.浓硫酸腐蚀衣物和皮肤是物理变化
3.实验室中常需要使用硫酸。(1)用小木棍蘸少量浓硫酸,放置一会儿后,可观察到____________________。(2)98%的浓硫酸稀释为稀硫酸时,一定要将_______沿烧杯壁缓慢地注入盛有____的烧杯里,并用________搅拌,此时若用手轻轻触碰烧杯外壁,有__________的感觉。
盐酸能与哪些物质发生化学反应
2.向分别盛有镁条、碳酸钠粉末、生锈铁钉、硝酸银溶液、氯化钡溶液的5支试管中各加入少量稀盐酸。
试着自己写一下相关反应的化学方程式。
看看你写的化学方程式正确吗?
Na2CO3+2HCl
NaCl+H2O+CO2↑
2FeCl3+3H2O↑
盐酸不能与氯化钡溶液发生反应。
除锈后的铁钉能不能继续与盐酸反应,如果能请你尝试写出反应的化学方程式。
除锈后的铁钉能继续与盐酸反应:Fe+2HCl FeCl2+H2↑
【例3】用足量的盐酸浸泡生锈的铁钉,可观察到的实验现象是( )①铁钉上的铁锈消失 ②铁钉上有气泡产生 ③溶液呈棕黄色A.只有①② B.只有①③ C.只有③ D.①②③
铁锈消失、溶液呈棕黄色
铁锈完全反应后继续加盐酸
实验时,李华把一枚生锈的铁钉放入足量的稀盐酸中,过一会儿,他看到的现象是____________________________;发生反应的化学方程式为______________________________;过一段时间,他又看到铁钉表面有气泡产生,该反应的化学方程式为____________________________。他又将铝片放入足量的稀盐酸中,奇怪的是开始无明显现象,过一段时间后才看到有气泡冒出,试用学过的知识解释原因_____________________________,_____________________________ (用化学方程式表示)。
2Al+6HCl===2AlCl3+3H2↑
铁锈逐渐消失,溶液变成黄色
Fe2O3+6HCl===2FeCl3+3H2O
Fe+2HCl===FeCl2+H2↑
Al2O3+6HCl===2AlCl3+3H2O
生产化肥、农药、火药以及染料
实验室中常用它做干燥剂
浓盐酸:有挥发性,应密封保存
稀释:将浓硫酸沿器壁慢慢倒入水中,并不断搅拌
盐酸:用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;
硫酸:用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属防锈等;
酸能使紫色石蕊试液变红,不能使无色酚酞试液变色。
金属镁、碳酸钠、铁锈(主要成分是氧化铁)、硝酸银溶液都能在常温下与盐酸发生反应
鲁教版九年级下册第一节 酸及其性质示范课ppt课件: 这是一份鲁教版九年级下册第一节 酸及其性质示范课ppt课件,共16页。PPT课件主要包含了Contents,盐与复分解反应,酸的通性,课堂小结等内容,欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质课堂教学ppt课件: 这是一份初中化学鲁教版九年级下册第一节 酸及其性质课堂教学ppt课件,共40页。PPT课件主要包含了生活中有酸味的物质,认识浓盐酸和浓硫酸,浓盐酸,浓硫酸,浓硫酸具有吸水性,猜一猜,浓硫酸具有脱水性,木棍变黑,什么是酸,酸的化学性质等内容,欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质教案配套课件ppt: 这是一份初中化学鲁教版九年级下册第一节 酸及其性质教案配套课件ppt,共32页。PPT课件主要包含了H+和酸根离子,酸的定义,浓硫酸的特性,浓硫酸的稀释等内容,欢迎下载使用。













